

胆管癌靶向药物Tibsovo获批 无进展生存期翻倍
2021-08-31来源:厚朴方舟
胆管癌是一种侵袭性较强且预后较差的恶性肿瘤,自2020年4月,胆管癌靶向药Pemazyre(培米替尼)率先获美国 FDA 批准上市后,胆管癌的靶向治疗也迎来了突破性进展。今年8月25日,FDA批准另一款靶向治疗药物Tibsovo(ivosidenib)用于治疗携带IDH1突变的局部晚期或转移性胆管癌成人患者,成为头个获批用于治疗这一患者群体的靶向治疗,为胆管癌的治疗贡献更多的治疗选择。

▲图源:参考文献[1]
胆管癌靶向治疗无进展生存期成倍延长
此次Tibsovo(ivosidenib)的获批是基于ClarIDHy临床试验数据的支持,这是头一个针对IDH1突变胆管癌患者的随机3期临床试验。研究结果显示:
●Tibsovo将疾病进展和死亡风险降低63%;
●与对照组相比,Tibsovo延长中位无进展生存期近一倍(Tibsovo组为2.7个月,对照组为1.4个月),32%的患者在治疗6个月时仍保持无进展或死亡,22%的患者在治疗1年后仍保持无进展或死亡;
●总生存期也显著延长(Tibsovo总生存期为10.3个月,对照组为7.5个月)[1]。
Tibsovo(ivosidenib)是一款针对IDH1 基因突变癌症的强效口服靶向抑制剂。IDH1 是一种代谢酶,其基因突变存在于包括急性髓系白血病、胆管癌和神经胶质瘤在内的多种肿瘤。
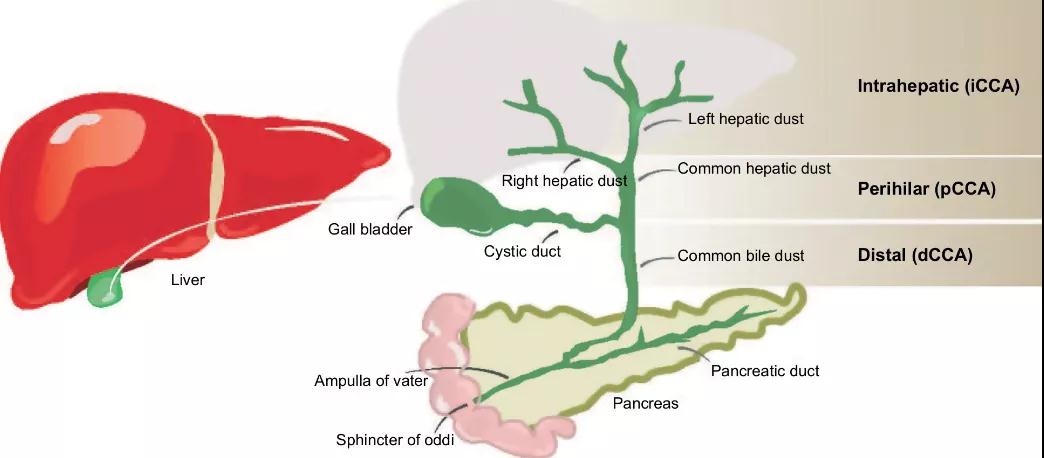
▲图源:dovepress
胆管癌靶向治疗进展
除了已经获批的Pemazyre(用于先前已接受过治疗、存在FGFR2融合或重排、不能手术切除的局部晚期或转移性胆管癌,延长生存期近3倍)、Truseltiq(用于已接受过治疗、携带FGFR2融合或重排的局部晚期或转移性胆管癌,缓解率提高一倍以上)以及Tibsovo外,还有不少胆管癌靶向药物正在临床试验中,也取得了显著的效果。相关阅读:胆管癌五款靶向治疗药物新进展,延长生存期三倍以上
Futibatinib:评估futibatinib治疗携带FGFR2基因重排(包括基因融合)、接受过至少一种治疗失败的局部晚期或转移性肝内胆管癌(iCCA)患者的临床试验结果显示:futibatinib治疗的缓解率(ORR)为41.7%;疾病控制率(DCR)为82.5%;中位无进展生存期(PFS)为9.0个月、中位总生存期(OS)为21.7个月,72%的患者在12个月时存活[2]。
Anlotinib+TQB2450:2021年美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO-GI)中,研究人员公布了使用Anlotinib与PD-L1单抗TQB2450的用药组合治疗胆管癌的效果数据:缓解率为37.5%,疾病控制率为70.8%。
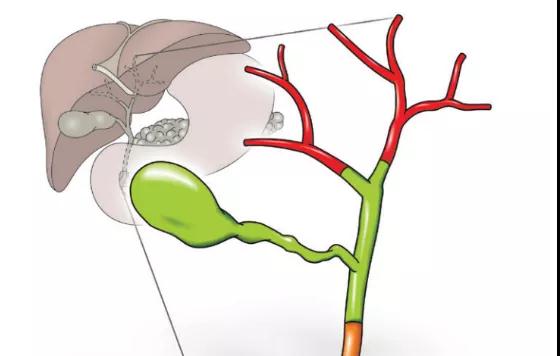
▲图源:cholangiocarcinoma
越来越多的证据证实,针对恶性程度极高的胆管癌,采用分子靶向治疗的效果更为显著。此次Tibsovo的获批为胆管癌患者提供了新的治疗选择,大幅延长了患者的生存期。厚朴方舟作为国内知名海外医疗服务机构,与日本、美国、英国等100多家权威医院有着深入的合作关系,可以为有需要的患者提供世界先进的治疗方案。如希望了解更多胆管癌先进治疗方案,可拨打热线400-086-8008联系我们。
参考文献:
[1] Servier Announces FDA Approval of TIBSOVO® (ivosidenib tablets) in IDH1-Mutated Cholangiocarcinoma
https://www.prnewswire.com/news-releases/servier-announces-fda-approval-of-tibsovo-ivosidenib-tablets-in-idh1-mutated-cholangiocarcinoma-301363055.html
[2] Taiho Oncology Announces Presentation of Phase 2 Data for Futibatinib (TAS-120) in Advanced Intrahepatic Cholangiocarcinoma at Virtual AACR Annual Meeting 2021
[3] FDA approves third oncology drug that targets a key genetic driver of cancer, rather than a specific type of tumor
https://www.prnewswire.com/news-releases/fda-approves-third-oncology-drug-that-targets-a-key-genetic-driver-of-cancer-rather-than-a-specific-type-of-tumor-300902681.html
[4] 美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO-GI)
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
上一篇:延长早期肺癌生存期,降低复发风险34%的免疫药物获FDA优先审查 下一篇:头款降低乳腺癌复发风险的靶向药已获FDA优先审评资格
相关推荐
厚朴方舟
厚朴方舟出国看病机构是中国企业初个拥有日本政府颁发的国际医疗从业资格证的公司,多年来整合了全球权威医疗资源,一直致力于打造“以患者为中心”的专业就医服务平台。公司在北京,上海,日本,美国均有分公司,为客户提供一站式海外就医服务。

咨询热线:400-086-8008
互联网药品信息服务资格证书编号:
(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号 京公网安备 11010502027115号