

2022年8月国际癌症治疗进展,治疗乳腺癌、肺癌、前列腺癌等多款新药获批
2022-09-08来源:厚朴方舟
2022年8月国际上癌症治疗领域全面开花,多款创新癌症治疗药物获得批准,可应用于临床。今天厚朴方舟为大家整理了8月癌症领域上市的新药,希望能为癌症患者提供些许帮助。
▲图源:everydayhealth
一、乳腺癌
1、初个HER2低表达乳腺癌靶向药物诞生
8月5日,美国FDA批准 Enhertu (T-DXd,DS-8201)新适应症,用于治疗无法切除或转移性HER2低表达(HER2-low)乳腺癌患者,这是初个获批用于HER2低表达乳腺癌亚型患者的药物。
▲图源:参考来源[2]
此项批准主要基于III期试验DESTINY-Breast04的数据。结果显示,与标准治疗相比,无论HR状态如何,采用Enhertu治疗后,患者的无进展生存期和总生存期均显著延长。具体数据为:
在HR阳性队列中,Enhertu将患者疾病进展或死亡风险降低49%,中位无进展生存期为10.1个月,对照组为5.4个月;将死亡风险降低了36%,中位总生存期达到23.9个月,对照组仅为17.5个月;
在全体患者中,Enhertu将患者疾病进展或死亡风险降低50%,中位无进展生存期为9.9个月,对照组为5.1个月;将死亡风险降低了36%,中位总生存期达到23.4个月,对照组仅为16.8个月;
在HR阴性队列中,Enhertu将患者疾病进展或死亡风险降低54%,中位无进展生存期为8.5个月,对照组为1.9个月;将死亡风险降低了52%,中位总生存期达到18.2个月,对照组仅为8.3个月。
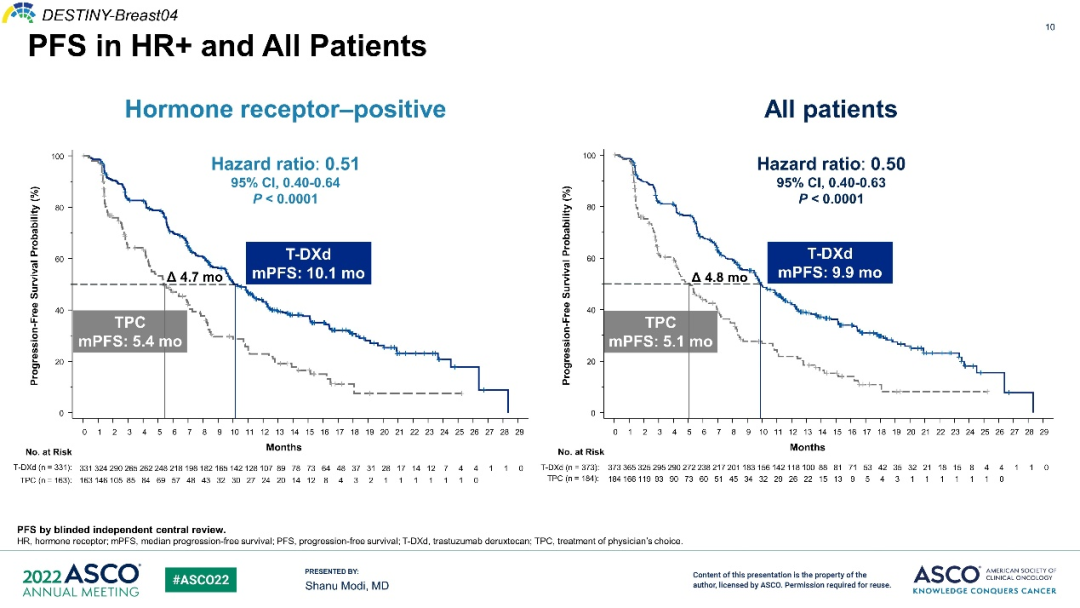
▲图源:2022 ASCO年会
2、乳腺癌初款辅助靶向药物获欧盟批准
8月4日,欧盟委员会(EC)批准PARP抑制剂Lynparza(olaparib,奥拉帕利)作为单药或与内分泌治疗联合,用于曾接受过新辅助治疗或辅助化疗的、携带种系BRCA突变(gBRCAm)的高风险HER2阴性早期乳腺癌患者。

▲图源:参考来源[5]
此次批准是基于OlympiA试验的积极结果,相关结果已于2021年6月发表在《新英格兰医学杂志》上。研究结果显示Lynparza能够显著降低高危患者乳腺癌复发的风险。具体数据为,Lynparza将侵袭性乳腺癌复发、继发癌症或死亡的风险降低了42%,将患者死亡风险降低32%。在随访3年后,Lynparza组的乳腺癌患者中有85.9%的人群仍然存活且未出现乳腺癌的复发,对照组仅为77.1%。
二、肺癌
1、肺癌初个HER2靶向药物获FDA加速批准
8月11日,美国FDA宣布抗体偶联药物(ADC)Enhertu(DS-8201,T-DXd)扩展适应症,用于治疗此前接受过一种系统性治疗的,携带激活性HER2突变的无法切除或转移性非小细胞肺癌(NSCLC)患者。Enhertu成为用于HER2突变非小细胞肺癌的初款药物。

▲图源:参考来源[1]
此次FDA加速批准是基于临床试验DESTINY-Lung02的积极结果。研究纳入了52名既往全身治疗后出现疾病进展的不可切除或转移性HER2突变非鳞状非小细胞肺癌患者。新数据显示,Enhertu治疗HER2阳性非小细胞肺癌的缓解率(ORR)为58%,中位缓解持续时间(DOR)为8.7个月。
三、前列腺癌
1、靶向联合雄激素剥夺治疗获FDA批准
8月8月,美国FDA已批准口服雄激素受体抑制剂(ARi)Nubeqa (darolutamide,达罗他胺)联合多西他赛的补充新药申请(sNDA),用于转移性激素敏感性前列腺癌(mHSPC)患者的治疗,为前列腺癌患者提供了新的治疗方向[6]。

▲图源:参考来源[6]
这一优先审评资格基于一项关键性3期ARASENS临床试验的积极结果。研究结果显示,与对照组(ADT+多西他赛)相比,Nubeqa+多西他赛+ADT的联合治疗显著延长了前列腺癌患者的生存期。具体数据为,接受Nubeqa+多西他赛+ADT的联合治疗的前列腺癌患者4年总生存率显著增长(62.7% vs 50.4%),降低死亡风险32.5%,中位治疗持续时间增长一倍以上(41.0个月 vs 16.7个月)[7]。
以上就是8月获批的抗癌药物,除此之外,9月也将有更多新药获批于临床,如FDA将在9月30日前对用于治疗携带FGFR2基因重排(包括基因融合)的局部晚期或转移性胆管癌的选择性不可逆FGFR1、2、3、4口服小分子抑制剂futibatinib做出审批意见,有望为癌症等重疾患者带来新的治疗方向,显著延长患者的生存期。
对于备受癌症困扰的患者,寻找权威的医院及医生诊治,了解全球先进的治疗药物,或许可以找到更有效的、延长生存期的治疗方案。厚朴方舟作为海外医疗服务机构中的佼佼者,与美国、日本、英国100多家世界知名的癌症治疗中心有着深入的合作关系,已经为许许多多的癌症患者提供服务,帮助患者延长生存期。
如希望了解更多癌症治疗前沿资讯,或想预约癌症权威医院及专家诊治的朋友,可以拨打400-086-8008或在线联系医学顾问进行咨询。
参考来源:
[1]FDA grants accelerated approval to fam-trastuzumab deruxtecan-nxki for HER2-mutant non-small cell lung cancer | FDA
[2]FDA Approves First Targeted Therapy for HER2-Low Breast Cancer | FDA
[3]2022年美国临床肿瘤学会(ASCO)年会
[4]Trastuzumab Deruxtecan in Previously Treated HER2-Low Advanced Breast Cancer | NEJM
[5]LYNPARZA® (olaparib) Approved in the EU as Adjuvant Treatment for Patients With Germline BRCA-Mutated, HER2-Negative High-Risk Early Breast Cancer - Merck.com
[6]U.S. FDA approves additional indication of darolutamide in combination with docetaxel for the treatment of metastatic hormone-sensitive prostate cancer (mHSPC) - Bayer News
[7]Darolutamide and Survival in Metastatic, Hormone-Sensitive Prostate Cancer | NEJM
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
上一篇:2022年5月至7月新药盘点丨多款创新疗法获批,涉及食管癌、白血病、淋巴瘤、卵巢癌等 下一篇:美国癌症研究协会发布2022年抗癌进展:多款癌症新药获批,癌症死亡率下降32%!
相关推荐
厚朴方舟
厚朴方舟出国看病机构是中国企业初个拥有日本政府颁发的国际医疗从业资格证的公司,多年来整合了全球权威医疗资源,一直致力于打造“以患者为中心”的专业就医服务平台。公司在北京,上海,日本,美国均有分公司,为客户提供一站式海外就医服务。

咨询热线:400-086-8008
互联网药品信息服务资格证书编号:
(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号 京公网安备 11010502027115号