

三阴性乳腺癌多个创新治疗方法获批,生存期显著延长
2021-04-25来源:厚朴方舟
乳腺癌是女性常见的恶性肿瘤,2020年的数据指出,乳腺癌发病人数已超过肺癌。三阴性乳腺癌(TNBC)是指雌激素受体(ER)、孕激素受体(PR)、人表皮生长因子受体2(HER-2)判定为阴性的乳腺癌,约占所有乳腺癌的10%~15%。与其他乳腺癌类型预后效果较好不同,三阴性乳腺癌侵袭性强,极易发生远处转移以及局部位置的复发,整体的5年生存率仅为77%[2](乳腺癌整体5年生存率为90%[3])。另外,三阴性乳腺癌的临床治疗选择十分有限,主要治疗方法为化疗,因此迫切需要更有效的治疗方案。随着靶向治疗和免疫治疗等新型治疗方法在癌症治疗中的应用,靶向治疗和免疫治疗在三阴性乳腺癌中也显现出良好的效果,显著延长了患者的生存期。
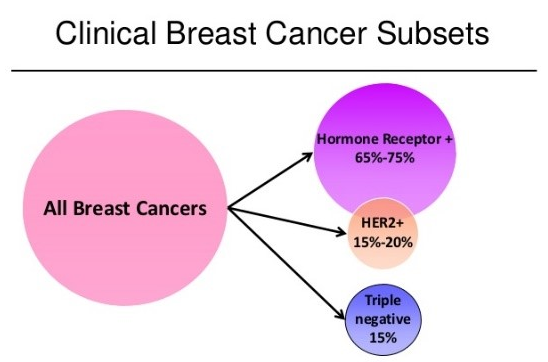
▲图源:komensandiego
头个提高三阴性乳腺癌无进展生存期和总生存期的治疗方法
4月7日,美国食品和药物管理局(FDA)已授予靶向抗癌药Trodelvy完全批准,用于治疗:先前已接受过至少2种治疗方法、其中至少1种治疗转移性疾病的不可切除性局部晚期或转移性三阴性乳腺癌(TNBC)成人患者。Trodelvy是头一个可提高三阴性乳腺癌患者无进展生存期(PFS)和总生存期(OS)的治疗方法,标志着三阴性乳腺癌治疗方面的一个重大进步。

▲图源:gilead
此次完全批准,基于3期ASCENT(NCT02574455)试验的结果,研究结果表明,与化疗相比,Trodelvy将无进展生存期显著延长(中位PFS:4.8个月 vs 1.7个月)、疾病进展或死亡风险显著降低57%、将总生存期显著延长(中位OS:11.8个月 vs 6.9个月)、死亡风险显著降低49%[4]。
头款三阴性乳腺癌免疫检查点抑制剂
2019年3月8日,FDA(美国食品和药物管理局)批准PD-L1单抗Atezolizumab(TECENTRIQ®)与紫杉醇结合蛋白的治疗方法,用于无法切除的局部晚期或具转移性,且肿瘤有明显的PD-L1表达的三阴性乳腺癌(TNBC)患者。Atezolizumab是全球头款用于治疗乳腺癌的免疫检查点抑制剂。
▲图源:FDA
此次批准基于IMpassion130(NCT02425891),研究结果表明,与对照组相比,Atezolizumab联合紫杉醇结合蛋白治疗,显著延长三阴性乳腺癌的无进展生存期(中位PFS:7.4个月vs4.8个月),将客观缓解率提高了20%(ORR:53%vs33%)。
Keytruda治疗三阴性乳腺癌效果显著
2020年11月,美国FDA已加速批准其重磅PD-1抑制剂Keytruda与化疗联用,用于经FDA批准的检测确定肿瘤表达PD-L1([CPS]≥10)的不可切除局部复发性或转移性三阴性乳腺癌(TNBC)患者。
▲图源:businesswire
此次加速批准是基于名为KEYNOTE-355的3期临床试验的结果,研究结果显示,Keytruda组与对照组相比,将疾病进展和死亡风险降低35%;无进展生存期显著延长(中位PFS:9.7个月vs5.6个月);缓解时间显著延长(中位DOR:19.3个月vs7.3个月)[6]。
除了与化疗联用可显著提高三阴性乳腺癌治疗的效果外,Keytruda单药作为手术后辅助治疗早期三阴性乳腺癌、单药治疗局部晚期或转移性三阴性乳腺癌均显现出良好的效果。
今年4月1日,Keytruda治疗接受过一线或二线系统治疗的三阴性乳腺癌患者的研究结果(KEYNOTE-119)发表在《柳叶刀·肿瘤》杂志上。研究结果显示,随着PD-L1表达水平的上升,化疗联用Keytruda的方案治疗的效果增强。在PD-L1 CPS≥10的TNBC患者群体中,Keytruda联合化疗显著延长了患者无进展生存期(中位PFS:9.7个月vs5.6个月)[7]。

▲图源:thelancet
另外,2020年2月发表在《The New England Journal of Medicine(NEJM)》的一项研究指出,Pembrolizumab联合化疗在未经治疗的Ⅱ期或Ⅲ期三阴性乳腺癌显现出良好的效果,完全缓解率比对照组高13.6%(64.8%vs51.2%)[8]。
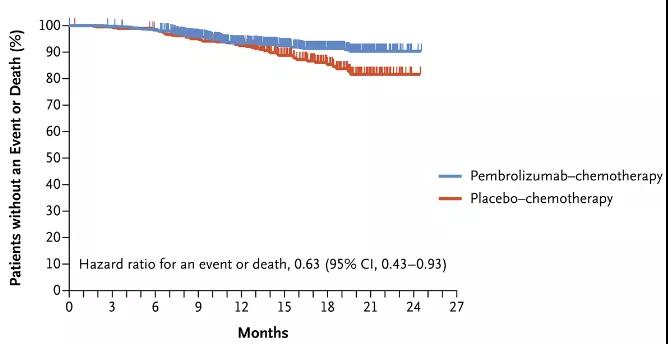
▲图源:NEJM
虽然三阴性乳腺癌的病情十分凶险,但研究人员还是在努力发掘抑制它的方法,目前已有不少成果披露,显著延长了患者的生存期。所以对于乳腺癌患者而言,积极的配合治疗,不主动放弃,才会出现各种新的可能。如希望了解更多有关三阴性乳腺癌治疗方案,可拨打热线400-086-8008联系我们。
参考来源:
[1] 世界卫生组织国际癌症研究机构
https://www.iarc.fr/faq/latest-global-cancer-data-2020-qa/
[2] Triple Negative Breast Cancer Outlook: Survival Rates
https://www.healthline.com/health/triple-negative-breast-cancer-outlook-survival-rates-stage#survival-rates
[3] Survival Rates for Breast Cancer
https://www.cancer.org/cancer/breast-cancer/understanding-a-breast-cancer-diagnosis/breast-cancer-survival-rates.html
[4] FDA Approves Trodelvy®, the First Treatment for Metastatic Triple-Negative Breast Cancer Shown to Improve Progression-Free Survival and Overall Survival
[5] FDA approves atezolizumab for PD-L1 positive unresectable locally advanced or metastatic triple-negative breast cancer
[6] FDA Approves Merck’s KEYTRUDA® (pembrolizumab) in Combination With Chemotherapy for Patients With Locally Recurrent Unresectable or Metastatic Triple‑Negative Breast Cancer Whose Tumors Express PD-L1 (CPS ≥10)
[7] Pembrolizumab versus investigator-choice chemotherapy for metastatic triple-negative breast cancer (KEYNOTE-119): a randomised, open-label, phase 3 trial
[8] Pembrolizumab for Early Triple-Negative Breast Cancer
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
上一篇:2020年全球肺癌手术治疗新进展 下一篇:神经系统疾病诊断利器--7T-MRI,准确诊治神经系统疾病
相关推荐
厚朴方舟
厚朴方舟出国看病机构是中国企业初个拥有日本政府颁发的国际医疗从业资格证的公司,多年来整合了全球权威医疗资源,一直致力于打造“以患者为中心”的专业就医服务平台。公司在北京,上海,日本,美国均有分公司,为客户提供一站式海外就医服务。

咨询热线:400-086-8008
互联网药品信息服务资格证书编号:
(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号 京公网安备 11010502027115号