

美国治疗注意力缺陷/多动障碍(ADHD)新药-Strattera(阿托西汀)
2017-08-30来源:厚朴方舟
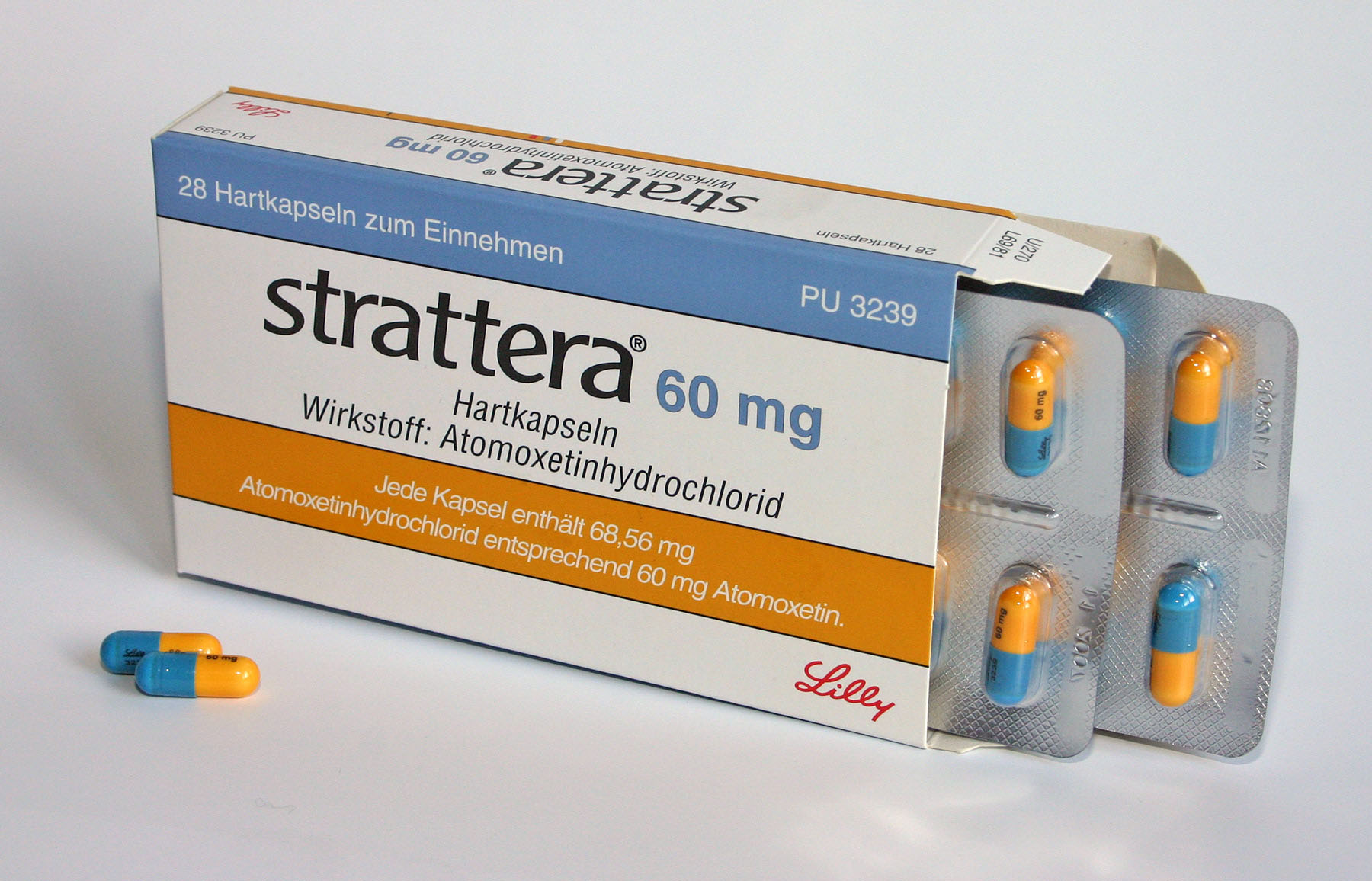
美国食品和药物管理局近期批准了前列个通用版本的Strattera(阿托西汀)治疗小儿和成人患者的注意力缺陷/多动障碍(ADHD)。
Apotex Inc.,Teva Pharmaceuticals USA Inc.,Aurobindo Pharma Limited和Glenmark Pharmaceuticals Limited今天获得批准,以多重优势推广阿托莫西汀。
美国FDA药物评估和研究中心通用药物办公室主任Kathleen Uhl说:“今天的批准标志着向消费者提供符合FDA严格标准的额外治疗方法的重要一步。“快速将仿制药推向市场,使患者有更多的选择来治疗他们的病情是FDA的首要任务。”
FDA批准的通用处方药与品牌药物具有相同的高品质和强度。通用处方药制造和包装场所必须通过与品牌药物相同的质量标准。
ADHD标志着干扰功能或发育的不注意和/或多动 - 冲动的持续模式。
在儿童和青少年阿托西汀的临床试验中,报告的较常见的副作用是胃不舒服,食欲降低,恶心或呕吐,头晕,疲劳和情绪波动。在成年人的临床试验中,报告的较常见的副作用是便秘,口干,恶心,食欲降低,头晕,性副作用,以及通过尿液的问题。
艾莫西汀必须放弃描述药物使用和警告的患者药物指南。这种药物有一个盒装警告,指出儿童和青少年自杀意念的风险增加。应该适当监测服用这种药物的患者,特别是在药物治疗过程的较初几个月,或剂量变化时,临床恶化,自杀和行为异常变化密切观察。其他重要的警告包括严重的肝脏损害和心血管事件严重的危险。
美国食品和药物管理局(FDA)是美国卫生与人类服务部的一个机构,通过确保人类和兽药,疫苗和其他人类生物制品以及医疗器械的不受威胁性,有效性和不受威胁性来保护公众健康。该机构还负责我国食品供应,化妆品,膳食补充剂,发出电子辐射的产品和烟草制品的不受威胁和保障。
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
上一篇:美国治疗丙型肝炎新药-Mavyret 下一篇:美国治疗巨细胞性动脉炎药物-FDA批准首批药物专门治疗巨细胞性动脉炎
相关推荐
厚朴方舟
厚朴方舟出国看病机构是中国企业初个拥有日本政府颁发的国际医疗从业资格证的公司,多年来整合了全球权威医疗资源,一直致力于打造“以患者为中心”的专业就医服务平台。公司在北京,上海,日本,美国均有分公司,为客户提供一站式海外就医服务。

咨询热线:400-086-8008
互联网药品信息服务资格证书编号:
(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号 京公网安备 11010502027115号