

2023美国靶向药新进展-去美国治疗癌症
2023-10-12来源:厚朴方舟
由于美国医疗技术先进,可供患者选择的新药更多,越来越多的患者为寻求更好的医疗而选择去美国治疗癌症等重疾。近日,美国癌症研究协会(AACR)发布了2023年抗癌进展报告(AACR Cancer Progress Report 2023),报告指出,从2022年8月1日到2023年7月31日,美国FDA共批准14款靶向治疗,9款免疫治疗及2款光学成像剂。
相关阅读:美国看病-日本看病=出国看病患者真实案例-厚朴方舟

其中,FDA批准的14款靶向治疗,涵盖范围包括肺癌、乳腺癌、卵巢癌、胆管癌等多种癌症治疗领域。
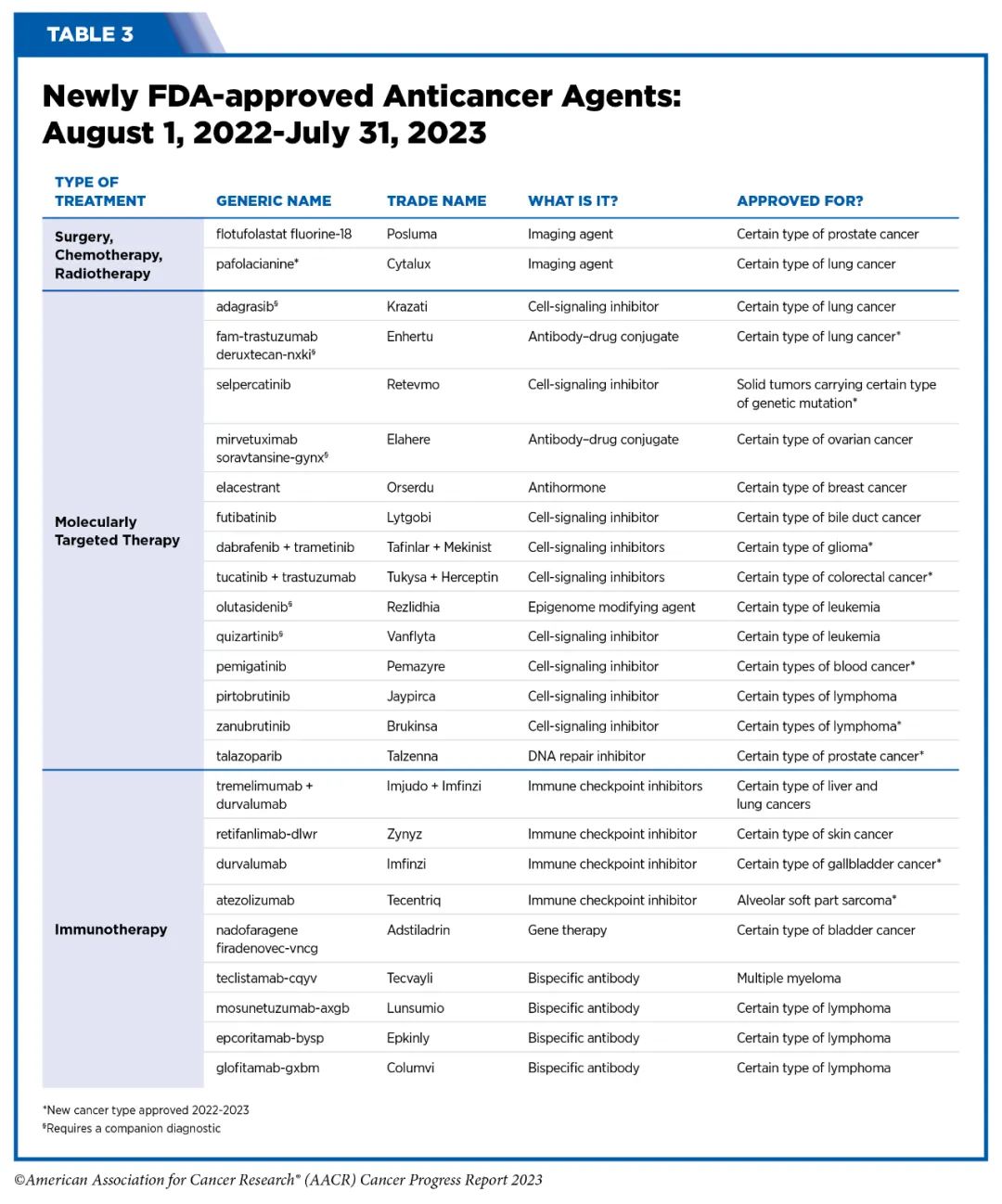
▲2022年8月-2023年7月FDA批准的创新抗癌方案,图源:参考来源[1]
一、第二款用于肺癌的KRAS靶向药Krazati
2022年12月,美国FDA宣布加速批准KRAS G12C抑制剂Krazati(Adagrasib)上市,用于治疗先前至少接受过一种全身性治疗的、携带KRAS G12C突变的局部晚期或转移性非小细胞肺癌(NSCLC)患者,Krazati成为第二款用于肺癌的KRAS靶向药。
2022 ASCO年会中公布的数据显示,Adagrasib单药或作为联合治疗用于KRAS G12C突变晚期或转移性非小细胞肺癌患者的客观缓解率(ORR)为42.9%,疾病控制率(DCR)为79.5%;中位缓解持续时间(DoR)为8.5个月,中位无进展生存期(PFS)为6.5个月,中位总生存期(OS)为12.6个月。
二、率先获批用于HER2突变非小细胞肺癌的靶向药物Enhertu
2022年8月,美国FDA宣布抗体偶联药物(ADC)Enhertu(DS-8201,T-DXd)扩展适应症,用于治疗此前接受过一种系统性治疗的,携带激活性HER2突变的无法切除或转移性非小细胞肺癌(NSCLC)患者[4]。Enhertu成为率先获批用于HER2突变非小细胞肺癌的靶向药物。
DESTINY-Lung02研究结果显示,Enhertu治疗HER2阳性非小细胞肺癌的缓解率(ORR)为58%,中位缓解持续时间(DOR)为8.7个月。
三、新一款不限癌症的靶向药物Retevmo
2022年9月,美国FDA已加速批准Retevmo(selpercatinib)扩展适应症,不限癌种治疗携带RET基因融合的局部晚期或转移性实体瘤患者,包括肺癌、胰腺癌、结直肠癌等实体瘤。
关键性临床试验LIBRETTO-001纳入了41名RET基因融合的实体瘤患者,包括胰腺癌、结直肠癌、唾液腺癌等多种癌症类型,在所有入组的患者中,90%的患者先前已经接受过全身治疗。
研究结果显示,Retevmo治疗RET基因融合的实体瘤患者总缓解率为44%,中位缓解持续时间为24.5个月,67%的患者缓解持续时间超过6个月。且不同癌症类型的患者缓解率不同,胰腺癌患者的缓解率为55%,结直肠癌为20%,唾液腺癌为44%。
四、难治性卵巢癌靶向药物Elahere
美国FDA已加速批准其靶向叶酸受体α(FRα)的抗体偶联药物(ADC)Elahere(mirvetuximab soravtansine)上市,作为单药治疗,治疗FRα高表达、对含铂治疗耐药的经治晚期卵巢癌患者。
此次Elahere的获批是基于关键性3期临床试验SORAYA的结果,该研究纳入了106例肿瘤表达高水平FRα的含铂药物耐药卵巢癌患者,其中51%的患者曾接受3线治疗,48%的患者曾接受1-2线治疗,48%的患者曾接受PARP抑制剂治疗。
研究结果显示,无论既往治疗的情况如何,Elahere对铂耐药卵巢癌患者均显现出突出的作用。具体数据为,Elahere治疗的客观缓解率为31.7%,中位缓解持续时间 (DOR) 为6.9个月。在今年ASCO年会中公布的数据显示,Elahere治疗的中位总生存期为13.8个月[7]。
五、率先获批的ESR1靶向药Orserdu
2023年1月,1月,美国FDA已批准Orserdu(Elacestrant)用于治疗患有雌激素受体阳性(ER+)、人表皮生长因子受体2阴性(HER2-)、ESR1突变的晚期或转移性乳腺癌的绝经后妇女或成年男子,这些患者在接受过至少一线内分泌治疗后出现疾病进展。Orserdu成为率先获批针对带有ESR1突变的ER+/HER2-晚期或转移性乳腺癌患者的治疗[8]。
本次Orserdu获批是基于3期EMERALD试验的研究结果,研究结果显示,与标准治疗(SOC)相比,Elacestrant使携带ESR1突变的乳腺癌患者的无进展生存率显著提升,具体数据为:
在ESR1突变的患者中,Elacestrant治疗的6个月无进展生存率为40.8%(对照组为19.1%),12个月无进展生存率为26.8%(对照组为8.2%);中位无进展生存期为8.6个月(对照组为1.9个月)。
六、胆管癌的FGFR靶向药物Lytgobi
2022年10月,美国FDA已加速批准Lytgobi(futibatinib)上市,用于治疗携带FGFR2基因融合或其它重排的不可切除、局部晚期或转移性肝内胆管癌经治成人患者。
Futibatinib通过与FGFR1-4的ATP结合“口袋”不可逆地共价结合,抑制FGFR介导的信号传导,从而降低携带FGFR1-4变异的肿瘤细胞的增殖。此次批准主要是基于2期FOENIX-CCA2研究结果。
2022年美国临床肿瘤学会(ASCO)年会中公布的研究结果显示,Futibatinib治疗的缓解率为41.7%,疾病控制率(DCR)为82.5%,中位缓解持续时间(DOR)为9.5个月,74%患者的缓解持续时间超过6个月,中位无进展生存期(PFS)为8.9个月,1年无进展生存率为35.4%;中位总生存期(OS)为20.0个月,1年生存率为73.1%[10]。
七、用于儿童低级别胶质瘤的Tafinlar+Mekinist双靶向治疗获批
2023年3月,美国FDA批准BRAF抑制剂Tafinlar(dabrafenib,达拉非尼)+MEK抑制剂Mekinist(trametinib,曲美替尼)的组合治疗,用于治疗1岁及以上需要全身治疗的BRAF V600E突变的低级别胶质瘤(LGG)儿童患者;FDA还批准了Tafinlar和Mekinist的液体制剂。
这标志着BRAF/MEK 抑制剂率先在小至一岁患者中应用,也使得Tafinlar+Mekinist成为率先获批用于治疗BRAF V600E LGG儿童患者的联合靶向治疗[11]。
FDA 批准 Tafinlar + Mekinist 是基于 II/III 期 TADPOLE 试验 (NCT02684058) 的结果。研究显示,Tafinlar/Mekinist与标准化疗相比,显著提高了携带BRAF V600变异的儿童低级别胶质瘤(LGG)患者的总缓解率,并降低患者疾病进展或死亡风险,有望为低级别胶质瘤患儿提供新的治疗标准。
具体数据为:Tafinlar/Mekinist治疗低级别脑胶质瘤的总缓解率为47%,而对照组仅为11%;Tafinlar/Mekinist组的中位无进展生存期(PFS)为20.1个月,而对照组仅为7.4个月,延长无进展生存期近三倍;采用Tafinlar/Mekinist治疗的患者肿瘤缩小或疾病稳定的概率为86%,而对照组仅为46%,近乎成倍增长。
八、针对HER2阳性结直肠癌患者的双靶向治疗获批
2023年1月,美国FDA加速批准其HER2抑制剂Tukysa(tucatinib),与HER2单克隆抗体Trastuzumab联用,治疗接受化疗后疾病出现进展的RAS野生型、HER2阳性无法切除或转移性结直肠癌患者,这是FDA率先批准针对HER2阳性结直肠癌的治疗。
此次批准是基于关键2期MOUNTAINEER 试验的结果。数据显示,客观缓解率达到38%,35%的患者部分缓解,3.6%的患者完全缓解[14]。此前ESMO(欧洲肿瘤内科学会)世界胃肠道肿瘤大会中公布的数据显示,中位缓解持续时间(DoR)为12.4个月,中位无进展生存期(PFS)为8.2个月,中位总生存期为24.1个月[13]。
九、针对IDH1突变急性髓性白血病的新药获批
2022年12月,美国FDA批准了Rezlidhia(olutasidenib)胶囊用于患有敏感性IDH1突变的复发性或难治性急性髓性白血病(AML)成人患者。
Rezlidhia是一种口服的小分子突变IDH1抑制剂,旨在结合并抑制突变的IDH1,以降低2-羟基戊二酸酯水平并恢复骨髓细胞的正常细胞分化。该药的获批为通常临床预后不佳的患者提供了一种新的口服治疗选择。
HEM-101(NCT0271957)研究结果显示,接受Rezlidhia治疗的患者完全缓解率(CR) +完全缓解伴部分血液学恢复(CRh)的比例为35%,其中完全缓解率为32%;完全缓解率(CR) +完全缓解伴部分血液学恢复(CRh)的中位总生存期为25.9个月 [14]。
十、创新靶向治疗使白血病患者缓解持续时间增长3倍
2023年7月,美国FDA批准FLT3抑制剂Vanflyta(quizartinib)联合标准化疗,以及作为巩固化疗后的维持性单药治疗,用于治疗经FDA批准检测方法证实带有FLT3-ITD突变阳性的新确诊急性髓细胞白血病(AML)成人患者。Vanflyta成为率先获得美国FDA批准用急性髓细胞白血病患者三个治疗阶段——诱导、巩固和维持治疗——的FLT3抑制剂。
QuANTUM-First临床3期试验结果显示,与标准治疗对照相比,接受Vanflyta联合标准诱导和巩固化疗治疗,然后继续接受Vanflyta单药治疗的新确诊的FLT3-ITD阳性患者,死亡风险降低22%。另外,虽然两组的完全缓解率相似,但接受Vanflyta单药治疗的患者中位完全缓解持续时间达到38.6个月,对照组仅为12.4个月,延长3倍以上。
十一、FGFR抑制剂获批用于髓系或淋巴系肿瘤
2022年8月美国FDA批准成纤维细胞生长因子受体(FGFR)抑制剂Pemazyre(pemigatinib)用于治疗带有 FGFR1 基因重组的复发或难治性髓系或淋巴系肿瘤(MLNs)成人患者。
这是Pemazyre获批的第二项适应症,它成为率先获批用于治疗带有 FGFR1 基因重组的MLN患者的精准治疗。
研究结果显示,采用Pemazyre治疗后完全缓解(CR)率为78%。
十二、套细胞淋巴瘤创新靶向药物Jaypirca获批
2023年1月,美国FDA加速批准了Jaypirca(pirtobrutinib),用于治疗至少两种系统治疗(包括布鲁顿酪氨酸激酶(BTK)抑制剂伊布替尼,acalabrutinib或泽布替尼)后复发或难治性套细胞淋巴瘤(MCL)的成年患者。
Jaypirca是FDA率先批准的也是仅有的一种非共价(可逆)BTK抑制剂。
十三、Brukinsa获批用于慢性淋巴细胞白血病或小淋巴细胞淋巴瘤
2023年1月,美国FDA已批准布鲁顿氏酪氨酸激酶(BTK)抑制剂Zanubrutinib(Brukinsa,泽布替尼)用于治疗慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL)成人患者。
研究结果显示,对于初诊的17p缺失慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL)成人患者采用Brukinsa的缓解率为88%;对于复发或难治性慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL)成人患者采用Brukinsa的缓解率为80%。
十四、创新PARP抑制剂降低前列腺癌死亡风险55%
2023年6月,美国FDA已批准口服PARP抑制剂Talzenna(他拉唑帕利,talazoparib)联合Xtandi(恩扎卢胺,enzalutamide)用于同源重组修复(HRR)基因变异的转移性去势抵抗性前列腺癌(mCRPC)成人患者的治疗。
Talzenna是率先获批与现有标准治疗(恩扎卢胺)联合用于HRR基因突变mCRPC成人患者的PARP抑制剂。临床试验数据显示,组合治疗可将HRR基因突变mCRPC患者的疾病进展或死亡风险降低55%。
以上就是2022年8月1日至2023年7月31日的12个月内,FDA批准的14款靶向治疗。由于篇幅有限,获得FDA批准的9款免疫治疗及2款光学成像剂将于明日发布。
总而言之,这些创新方案的不断进展在为患者提供更多治疗选择的同时,也显著提高了癌症患者的生存率。
未来,研究人员将继续瞄准精准医学,克服难治性靶点,为更多癌症患者带来新的、更有效的治疗方案,进一步提高患者的生存率。相信在不久的将来,癌症也将不再是令人“闻风丧胆”的“恶魔”,新一代的治疗技术将让更多癌症患者受益。
厚朴方舟作为国内海外医疗服务机构的佼佼者,与日本、美国、英国100多家权威癌症治疗中心有着深入的合作关系,可以为不幸罹患癌症的患者预约世界知名专家就诊,制定个体化治疗方案,并为患者提供一站式出国看病及远程会诊服务,有需要的朋友可以直接在线联系医学顾问或拨打免费热线400-086-8008联系我们。
参考来源:
[1]Cancer in 2023 | AACR Cancer Progress Report 2023
[2]Mirati Therapeutics Announces U.S. FDA Accelerated Approval of KRAZATI™
(adagrasib) as a Targeted Treatment Option for Patients with Locally Advanced or
Metastatic Non-Small Cell Lung Cancer (NSCLC) with a KRASG12C Mutation
[3]2022年美国临床肿瘤学会(ASCO)年会
[4]FDA grants accelerated approval to fam-trastuzumab deruxtecan-nxki for
HER2-mutant non-small cell lung cancer | FDA
[5]FDA Approves Lilly's Retevmo® (selpercatinib), the First and Only RET
Inhibitor for Adults with Advanced or Metastatic Solid Tumors with a RET Gene
Fusion, Regardless of Type
[6]ImmunoGen Announces FDA Accelerated Approval of ELAHERE™ (mirvetuximab
soravtansine-gynx) for the Treatment of Platinum-Resistant Ovarian Cancer |
Business Wire
[7]ImmunoGen Presents Additional Efficacy and Safety Analyses Evaluating
Mirvetuximab Soravtansine in Ovarian Cancer at ASCO | ImmunoGen, Inc.
[8]FDA approves elacestrant for ER-positive, HER2-negative, ESR1-mutated advanced or metastatic breast cancer | FDA
[9]FDA Approves Taiho's LYTGOBI® (futibatinib) Tablets for Previously
Treated, Unresectable, Locally Advanced or Metastatic Intrahepatic
Cholangiocarcinoma
[10]Taiho Oncology Announces Updated Efficacy and Safety Data for
Futibatinib in Cholangiocarcinoma at 2022 ASCO Annual Meeting
[11]Novartis Tafinlar + Mekinist approved by FDA for pediatric
[12]Seagen Announces FDA Accelerated Approval of TUKYSA® (tucatinib) in
Combination with Trastuzumab for People with Previously Treated RAS Wild-Type,
HER2-Positive Metastatic Colorectal Cancer | Business Wire
[13] Seagen - Seagen Announces TUKYSA® (tucatinib) in Combination with
Trastuzumab Granted Priority Review by FDA for Previously Treated HER2-Positive
Metastatic Colorectal Cancer
[14]FDA D.I.S.C.O. Burst Edition: FDA approval of Rezlidhia (olutasidenib)
for relapsed or refractory acute myeloid leukemia with a susceptible IDH1
mutation | FDA
[15]VANFLYTA® First FLT3 Inhibitor Approved in the U.S. Specifically for
Patients with Newly Diagnosed FLT3-ITD Positive AML | Business Wire
[16]Incyte Announces FDA Approval of Pemazyre® (pemigatinib) as the First
and Only Targeted Treatment for Myeloid/Lymphoid Neoplasms (MLNs) with FGFR1
Rearrangement | Incyte
[17]FDA grants accelerated approval to pirtobrutinib for relapsed or
refractory mantle cell lymphoma | FDA
[18]FDA approves zanubrutinib for chronic lymphocytic leukemia or small
lymphocytic lymphoma | FDA
[19]Pfizer’s TALZENNA® in Combination with XTANDI® Receives U.S. FDA Approval | Pfizer
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
上一篇:2023年第2版NCCN胃癌指南-胃癌海外就医新方案介绍 下一篇:2024年首版NCCN结直肠癌指南出炉!为直肠癌治疗揭开更精准的新篇章
相关推荐
厚朴方舟
厚朴方舟出国看病机构是中国企业初个拥有日本政府颁发的国际医疗从业资格证的公司,多年来整合了全球权威医疗资源,一直致力于打造“以患者为中心”的专业就医服务平台。公司在北京,上海,日本,美国均有分公司,为客户提供一站式海外就医服务。

咨询热线:400-086-8008
互联网药品信息服务资格证书编号:
(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号 京公网安备 11010502027115号